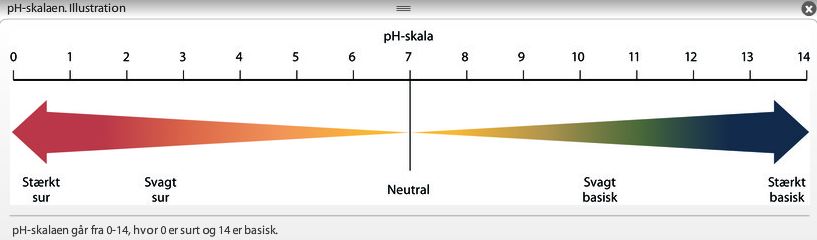
7.9 Hverdagsstoffers PH
7.12 Fortynding af en syre

Vi startede med at ligge 4 stykker indikatorpapirer ned på filterpapiret, og vi gav dem numrene fra 1-4. Derefter dyppede vi en glasspatel ned i flasken med saltsyre, og derefter satte vi en dråbe ned på nr. 1. Derefter hældte vi 9 mL vand ned i et literglas, og derefter kom vi 1 mL saltsyre i, og satte en dråbe ned på nr. 2. Herefter hældte vi 90 mL vand mere i glasset med saltsyre og vand, og satte en dråbe ned på nr. 3. Til sidst hældte vi så meget vand i at der var en liter, derefter satte vi en dråbe ned på nr. 4.
- PH-værdien stiger fra 1-7 og fra lilla til gul.
- Når man putter mere vand i bliver den mere neutral, ford
Punkt 1
Punkt 2:Neutral
Punkt 2:Neutral
Fremstilling af ammoniak og ammoniak vand(1)
I det forsøg skulle vi blande de to stoffer:Calciumhydroxid med den kemiske formel Ca(OH)_2, og Ammoniumchlorid med den kemiske formel NH_4CL.
- Punkt 1- Lugt til Calciumhydroxid: Det lugter ikke.
- Punkt 2- Lugt til Ammoiumchlorid: Det lugter ikke.
- Punkt 4- Lugt til blanding: Det lugter rigtig kraftig
- Farven på papiret er mørkegrøn/blå hvilket betyder at den er svag basisk.
7.16 Fremstilling af ammoniak og ammoniakvand(2)
Vi startede med at hælde 50 mL vand i et bægerglas. Så satte vi en prop med et glasrør igennem, som vi satte i et reagensglas med et reagensglas ovenpå på et stativ, som vi satte ind over bunsenbrænderen, hvor der var ild i. Da vi havde opvarmet reagensglasset satte vi det ned i bægerglasset.
- Punkt 1: Det som skete var at vandet skiftede til en rødlilla farve.
- Punkt 2: Det viser at ammoniakvand har meget nemt ved at blive opløst i vand.
- Punkt 3: Ammoniakvand er en base.
Ekstra-forsøg
Vi startede med at hælde 75 mL saltsyre(HCl) ned i et bægerglas, derefter hældte vi 30 mL ammoniakvand(NH_4OH) som er en base ned i et andet bægerglas. Derefter hældte vi 25 af de 75 mL saltsyre ned i et tredje bægerglas. Derefter satte vi en pH elektor til computeren ved hjælp af programmet Capstone, hvor man kan måle pH-værdier. Hver gang vi satte ektoren ned i ammoniakvandet steg pH-værdien, og den faldt hver gang vi satte den ned i saltsyren. Til sidst var pH-værdien på 7, og så kogte vi det indtil d3et blev til sammiak
7.7 En trylleblæk
Vi startede med at finde et bægerglas, noget natriumhydroxid(NaOH) og noget phenolphtalein. Derefter puttede vi 50 mL vand i bægerglasset, og så hældte vi 10 dråber phenolphtalein, og en lille smule natriumhydroxid ned i bægerglasset. Farven i glasset skiftede til lilla, og herefter puttede vi et par dråber ned på et hvidt viskestykke. Da pletten havde været der i noget tid begyndte den langsomt at forsvinde, og til sidst var den næsten helt væk. Pletten forsvinder fordi vandet optager carbondioxid(CO2) fra luften. CO2 reagerer med vandet og danner kulsyre CO2+H2O= H2CO3.
7.8 En tryllekunst
Vi startede med at finde 3 bægerglas, noget fortyndet saltsyre(HCl), noget fortyndet natriumhydroxid(NaOH) og noget phenolphtalein. I det første bægerglas, hældte vi vand og phenolphtalein i. I det andet glas hældte vi natriumhydroxid i, som er base. Og i det sidste glas hældte vi saltsyre i, som er syre. Derefter hældte vi væsken fra glas 1 ned i glas nr. 2, og herefter skiftede farven til helt rød, og derefter hældte vi væsken fra nr. 2, over i nr. 3, og nu stiftede farven til helt gennemsigtigt igen. Grunden til at det sker er fordi syre og base neutralisere hinanden, og man kan ikke drikke det fordi der er base deri.
7.14 Neutralisation af en syre
Vi startede med at finde indikatorpapir, en spatel, en vandfast tus, tre bægerglas, to plastsprøjter, bromthymolblåt(BTB), fortyndet saltsyre og fortyndet natriumhydroxid. Derefter hældte vi lidt saltsyre i det ene glas, og lidt natriumhydroxid i det andet. Det sidste glas, skulle vi bruge til at blande syre og base sammen i. Så vi hældte noget saltsyre fra glas 1 over i glas 3, og derefter tilsatte vi nogle dråber BTB-indikator. Væskens farve er nu gul. Herefter begyndte vi at drype noget natriumhydroxid ned i glasset, indtil væsken farve stiftede til grøn. Væskens ph-værdi er nu 7, og det betyder at væsken er blevet neutraliseret.