Forsøg med skumdannelse
Katalysatorer
Fællesforsøg: Forsøg med skumdannelse
Vi blandede ca. 50 mL brintoverilte(H2O2) med 5-10 mL sulfosæbe i et cylinderglas og stiller glasset på en avis.
Så hældte vi 10 mL kaliumiodidopløsning ned i blandingen og så hvordan der derefter væltede ud med gult skum.
Så satte vi en træpind med gløder ned på skummet, også kom der huller og den ikke slukkede, pga. at skummet indeholder O2. Kalium er katalysatoren, og den er metal. Reaktionen 2 H2O2--> 2 H2O+O2= 2 Brintoverilte--> 2 Vand+ Ilt
Vi blandede ca. 50 mL brintoverilte(H2O2) med 5-10 mL sulfosæbe i et cylinderglas og stiller glasset på en avis.
Så hældte vi 10 mL kaliumiodidopløsning ned i blandingen og så hvordan der derefter væltede ud med gult skum.
Så satte vi en træpind med gløder ned på skummet, også kom der huller og den ikke slukkede, pga. at skummet indeholder O2. Kalium er katalysatoren, og den er metal. Reaktionen 2 H2O2--> 2 H2O+O2= 2 Brintoverilte--> 2 Vand+ Ilt
Kobber som katalysator
En langsom hydrogenproduktion
Vi startede med at sætte tre reagensglas ned i et reagensglasstativ. Vi anbragte et zinkstykke i glas nummer 1. I glas nummer 2 anbragte vi et zinkstykke mere bare med et lille stykke tape rundt om. I det 3 glas anbragte vi en spatelfuld zinkpulver.
Derefter hældte vi lidt svovlsyre i alle glassene så de blev halvt fyldt. Det som sker når svovl syren kommer ned i glassene er at den fungerer som en katalysator, og den reagerer med zinken, så der dannes hydrogen, som så langsomt bobler op i glassene. Kobber er katalysatoren og det er også et metal. Reaktionen Zn(metal)+H2SO2(svovlsyre)-->H2(Hydrogen)+ZnSO4(salt(metal+syrerest))
Vi startede med at sætte tre reagensglas ned i et reagensglasstativ. Vi anbragte et zinkstykke i glas nummer 1. I glas nummer 2 anbragte vi et zinkstykke mere bare med et lille stykke tape rundt om. I det 3 glas anbragte vi en spatelfuld zinkpulver.
Derefter hældte vi lidt svovlsyre i alle glassene så de blev halvt fyldt. Det som sker når svovl syren kommer ned i glassene er at den fungerer som en katalysator, og den reagerer med zinken, så der dannes hydrogen, som så langsomt bobler op i glassene. Kobber er katalysatoren og det er også et metal. Reaktionen Zn(metal)+H2SO2(svovlsyre)-->H2(Hydrogen)+ZnSO4(salt(metal+syrerest))
Cigaretaske som katalysator
Vi startede med at tage en sukkerknald og satte den fast i en digeltang, som vi så førte ind over en bunsenbrænder, når man gør det kan man ikke få sukkeret til brænde. Fordi der ikke er ilt. Så tog vi en ny sukkerknald, men denne gang dryssede vi lidt cigaretaske ned på sukkeret, og gnider det lidt ind i overfladen. Derefter holder vi sukkeret ind i flammen. Og nu begynder det at brænde, fordi cigaretasken fungerer som en katalysator. Cigaretasken er katalysatoren, og det er et metal.
Cracking af paraffinolie
I dette forsøg skal vi lave cracking af paraffinolie altså brække paraffinolien i mindre dele, så det danner andre stoffer som er Benzin, propan og butan.
Vi startede med at fylde et cylinderglas op med vand, og så satte vi et reagensglas med en prop med to huller med to glasrør i i ned i cylinderglasset, derefter forbandt vi rørene med et andet reagensglas og en urinpose. i Det andet reagensglas kom vi i bunden 2-3 cm glasuld sammen med Paraffinolie og derefter 3-4 cm Perlekatalysator(så det er altså katalysatoren i det her forsøg) på toppen kom vi så glasolie. Det forsøget skal vise er at når man brækker paraffinolien i mindre stykker danner den andre stoffer som benzin, propan og butan. Farven af væsken i det første reagensglas er orange og det lugter rigtig dårligt. Gassen fra posen kan godt brænde.
Vi startede med at fylde et cylinderglas op med vand, og så satte vi et reagensglas med en prop med to huller med to glasrør i i ned i cylinderglasset, derefter forbandt vi rørene med et andet reagensglas og en urinpose. i Det andet reagensglas kom vi i bunden 2-3 cm glasuld sammen med Paraffinolie og derefter 3-4 cm Perlekatalysator(så det er altså katalysatoren i det her forsøg) på toppen kom vi så glasolie. Det forsøget skal vise er at når man brækker paraffinolien i mindre stykker danner den andre stoffer som benzin, propan og butan. Farven af væsken i det første reagensglas er orange og det lugter rigtig dårligt. Gassen fra posen kan godt brænde.
cracking af ethanol
I dette forsøg skal vi lave cracking af Ethanol.
Vi startede med at komme 2-3 cm glasuld ned i et reagensglas og derefter hældte 10 ml ethanol oveni. Så fyldte vi 4-5 cm perlekatalysator ned i og sluttede så med lidt glasuld til at lukke. Så satte vi en prop med et rør i i reagensglasset og førte det sammen med en urinpose via en slange. Så tænde vi for bundsenbrænderen, og satte reagensglasset ned over. Så lod vi det brænde indtil der kom nok gas i urinposen. Gassen som blev dannet er Ethen. Og ja gassen kan godt brænde. Man bruger ethen til at modne
Vi startede med at komme 2-3 cm glasuld ned i et reagensglas og derefter hældte 10 ml ethanol oveni. Så fyldte vi 4-5 cm perlekatalysator ned i og sluttede så med lidt glasuld til at lukke. Så satte vi en prop med et rør i i reagensglasset og førte det sammen med en urinpose via en slange. Så tænde vi for bundsenbrænderen, og satte reagensglasset ned over. Så lod vi det brænde indtil der kom nok gas i urinposen. Gassen som blev dannet er Ethen. Og ja gassen kan godt brænde. Man bruger ethen til at modne
N^2- fremstilling i laboratoriet til brug ved nH3- syntese
Vi startede med at putte noget ståluld ned i midten af et forbrændingsrør også satte vi to propper i hver ende.Derefter satte vi glasrør fast i propperne, og derefter fyldte vi en urinpose med luft, og en anden uden noget i. Begge poser satte vi sat i glasrørene. Så tændte vi ild til en bunsenbrænder, som skulle opvarme stålulden, også trykkede vi luften fra den ene pose over i den anden pose. Det gjorde at der kom gløder i ulden, fordi der er ilt tilstede. Luften fra posen er fyldt med Ilt(O2) og kvælstof N2. Når luften kommer ind til ulden sætter ilten så fast på ulden så den brænder, mens kvælstoffet kommer over i den anden pose, og tilbage til den første pose igen. I dette forsøg er det stålulden som er katalysatoren.
Ammoniakfremstilling:
Ammoniak er et af de kemikalier, hvoraf der fremstilles mest i verden.
Over 150 mio. tons, hvoraf langt størstedelen går til fremstilling af kunstgødning.
Fremstillingen af ammoniak kræver en forholdsvis stor varmetilførsel, og mere end 1% af verdens samlede energiforbrug går derfor til fremstillingen af ammoniak.
Råmaterialerne til industriel fremstilling af ammoniak, NH3 er dinitrogen (kvælstof), N2 og dihydrogen (brint), H2.
N2 fås fra den atmosfæriske luft, som indeholder 79 % N2.
H2 fremstilles industrielt ved reaktion mellem vand og enten kul eller kulbrinter fra olie og naturgas ved høj temperatur (8-900 0C).
Da vi lavede forsøget brugte vi ikke en katalysator, men vi brugte heller ikke kvælstof fra luften, eller brint fra kulbrinter. Vi brugte ammoniumchlorid og calciumhydroxid. Altså 2 kemiske forbindelser, men det vil være for dyrt i industrien.
Vi så ligeledes ved forsøget at Ammoniak er yderst glad for vand, og suger det til sig hvis det kan komme til det.
Ammoniakfremstilling:
Ammoniak er et af de kemikalier, hvoraf der fremstilles mest i verden.
Over 150 mio. tons, hvoraf langt størstedelen går til fremstilling af kunstgødning.
Fremstillingen af ammoniak kræver en forholdsvis stor varmetilførsel, og mere end 1% af verdens samlede energiforbrug går derfor til fremstillingen af ammoniak.
Råmaterialerne til industriel fremstilling af ammoniak, NH3 er dinitrogen (kvælstof), N2 og dihydrogen (brint), H2.
N2 fås fra den atmosfæriske luft, som indeholder 79 % N2.
H2 fremstilles industrielt ved reaktion mellem vand og enten kul eller kulbrinter fra olie og naturgas ved høj temperatur (8-900 0C).
Da vi lavede forsøget brugte vi ikke en katalysator, men vi brugte heller ikke kvælstof fra luften, eller brint fra kulbrinter. Vi brugte ammoniumchlorid og calciumhydroxid. Altså 2 kemiske forbindelser, men det vil være for dyrt i industrien.
Vi så ligeledes ved forsøget at Ammoniak er yderst glad for vand, og suger det til sig hvis det kan komme til det.
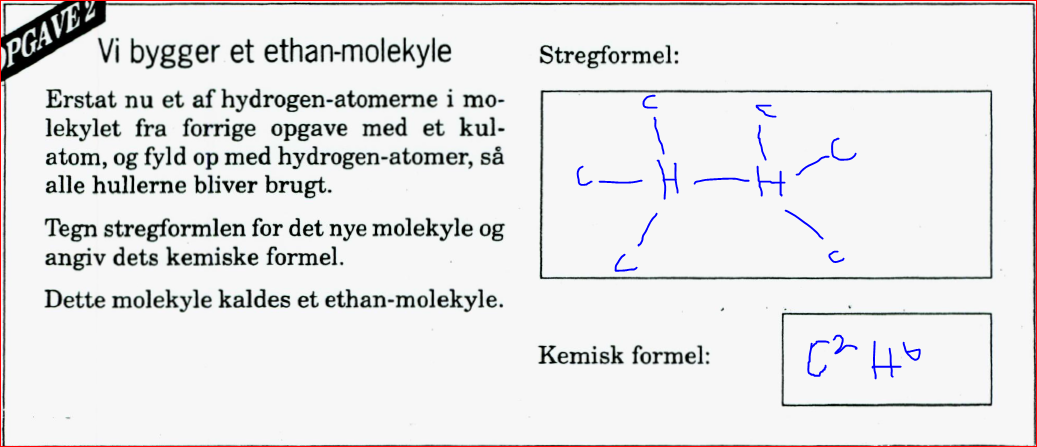
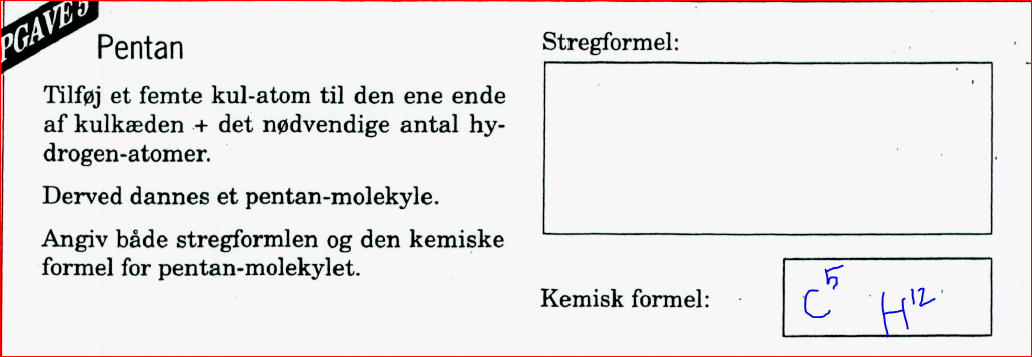
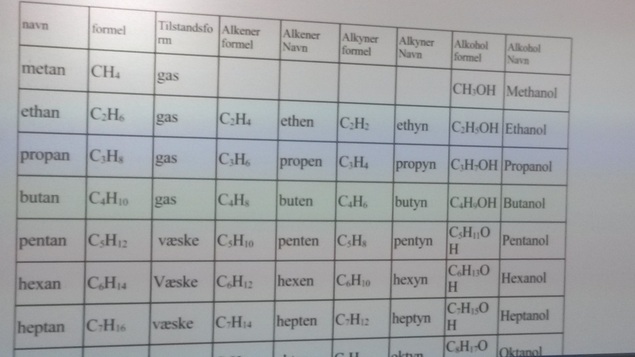
Ved fx Ethan sidder der ingen dobbelbinding mellem de to C-atomer. Men hvis fx ethen så er der en dobbelbindingen, og hvis det hedder Ethyn så er der en triblebindingen. Og hvis det hedder Ethanol, så er der en OH bindingen